質量パーセント濃度とモル濃度とは何か。また,硫酸銅5水和物(cuso4・ 5h2o)のような結晶水を含む固体を用いた場合,結晶水はどのように取り扱うのか?溶液調製に必要なポイン トを明示し て、「素人が読んでも理解できるよう」,簡潔に記してください。 という問題があるのですがわか質量パーセント濃度からモル濃度への変換も同じことである。 この場合、最初に1Lあるとして計算するとよい。 質量モル濃度の考え方 さて、3番目の質量モル濃度は、 (濃度)=(溶質)÷(溶媒) として計算するので、上記の2つの濃度とは考え方が違う。 しかし、単位の変換という点ではモル分率から質量パーセント濃度を求める方法を教えてください. 名前:芦田 実 日時:04年10月24日 17時10分00秒 かっしー 様 必ずしも専門家ではありませんので,不正確な回答もあります.教育学部から公開しているホームページの質問箱とQ&A集にも回答(一部)を載せたいと思います

2 117g G 500cm3 Descubre Como Resolverlo En Qanda
質量パーセント濃度 モル濃度
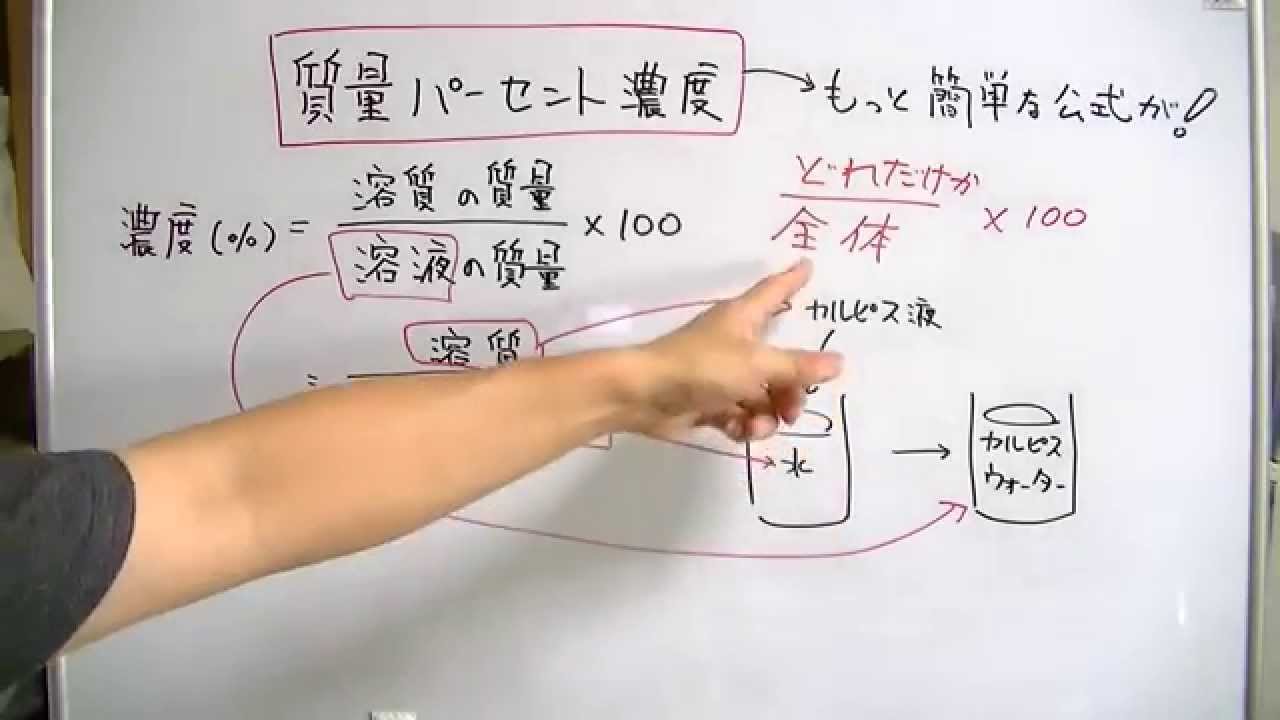
質量パーセント濃度 モル濃度-先ほどの質量パーセント濃度は、「g」を「g」で割ることによって求めましたね。 しかし、次に紹介するモル濃度は、少し様子が違います。 モル濃度とは、文字通り、モルで表した濃度のことです。 言い換えると、 「1Lあたりに、何molの物質が溶けているか」 ということです。 モル濃度〔mol/L 解答:1質量パーセント濃度2% 質 量 パ ー セ ン ト 濃 度 溶 質 溶 液 質 量 パ ー セ ン ト 濃 度 ( %) = 溶 質 ( g) 溶 液 ( g) × 100 問5 10molの水酸化ナトリウム (NaOH)を水に溶かして全体でLにしたときのモル濃度 (mol/L)を求めよ。 問5解答/解説




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット
「何g溶けているか」を表す方法が「質量パーセント濃度」であり,「何mol 溶けているか」を表す方法が「モル濃度」である. 「質量パーセント濃度」は小学校の算数で習うものなので,多くの学生は 計算方法を理解しているが,高校化学で登場する「モル濃度」になると,高 校化学履修者で濃度の変換問題は,質量パーセント濃度% ⇔ モル濃度mol/L の変換が頻出となる。 Ⅰ質量パーセント濃度に関する問題タイプ Ⅱモル濃度に関する問題タイプ ・質量パーセント濃度:溶液中に溶けている溶質の質量を百分率で表した濃度。溶液100gあたりの硝酸の質量パーセント濃度をモル濃度に変換します。 0 % 以上 9967 % 以下での誤差 (標準偏差)は ± mol/L です。
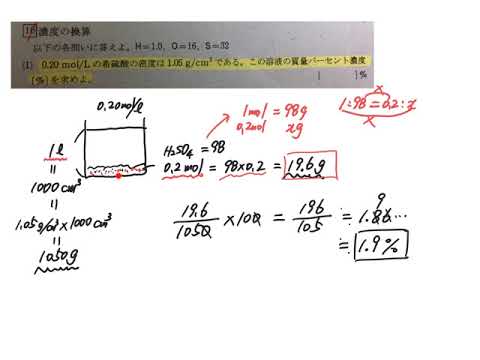
濃度を計算する問題 2組の入口へ 説明へGO 1 水酸化ナトリウムの結晶gを水80gに溶解させ、水酸化ナトリウム水溶液を作る。この水溶液の密度を12g/cm 3 とするとき、以の濃度を求めよ。 (原子量H=10,O=16,Na=23) 1,質量パーセント濃度 2,モル濃度は,質量体積パーセント濃度,若しくは質量容積パーセント濃度といい,分子が溶質 の質量 gで分母が溶液の体積mL の場合であり,w/v% = 溶質の質量g 溶液の体積mL ×100 で表す。 v/v% は,体積パーセント濃度といい, vol% という表し方もある。分子が溶質の体積mL で分母が溶液の体今、わかっていることは、質量パーセント濃度が98%ということと分子量が98ということと密度が18 g/cm 3 ということだが、モルはどこにも出てきていない!
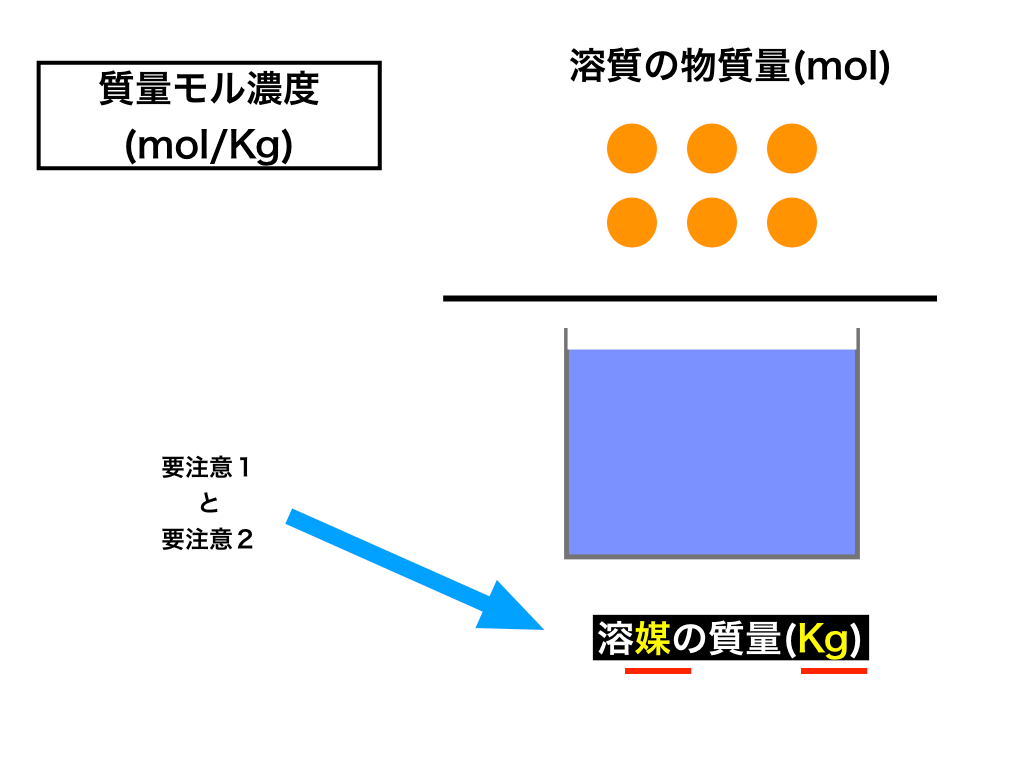
質量パーセント濃度と容量モル濃度 7 市販の濃硝酸は600%のHNO3 の水溶液で、密度が136 g/cm 3 である。この濃硝酸の容量モル濃度を求めよ。有 効数字3 桁 8 密度116 g/cm3 の塩酸はHCl を315%含む。この塩酸の容量モル濃度を求めよ。有効数字3 桁 9 市販の濃硫酸は密度が1 g/cm3 で、H2SO4 を960%含む モル濃度マスターへの道! ① もし物質 (mol)が分からなければ、物質量に変換してから溶液の体積 Lで割りましょう。 では今回は、モル濃度の問題の中でも密度が与えられて 「モル濃度から質量パーセント濃度へ変換せよ」 という問題について一緒に モル濃度では、溶液の体積L だったのに対し、 質量モル濃度では溶媒の質量kg です。 頻出の練習問題 質量パーセント濃度が98%の濃硫酸があり、その密度は25℃で1g/cm 3 である。




07溶液 モル濃度から質量モル濃度への単位変換 ポイント解説 4分 Youtube




化学 6回目授業 ブログ De 授業 21
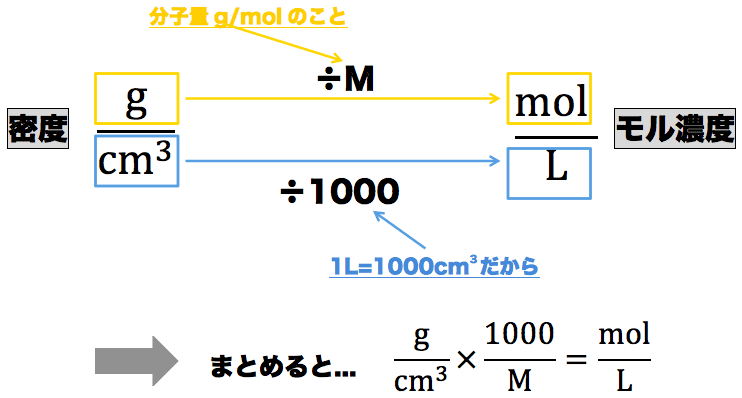
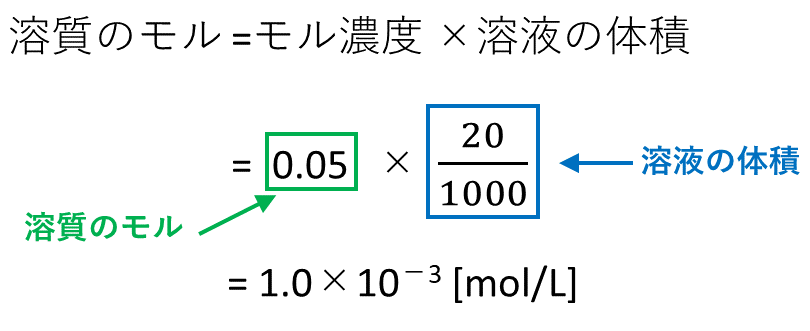
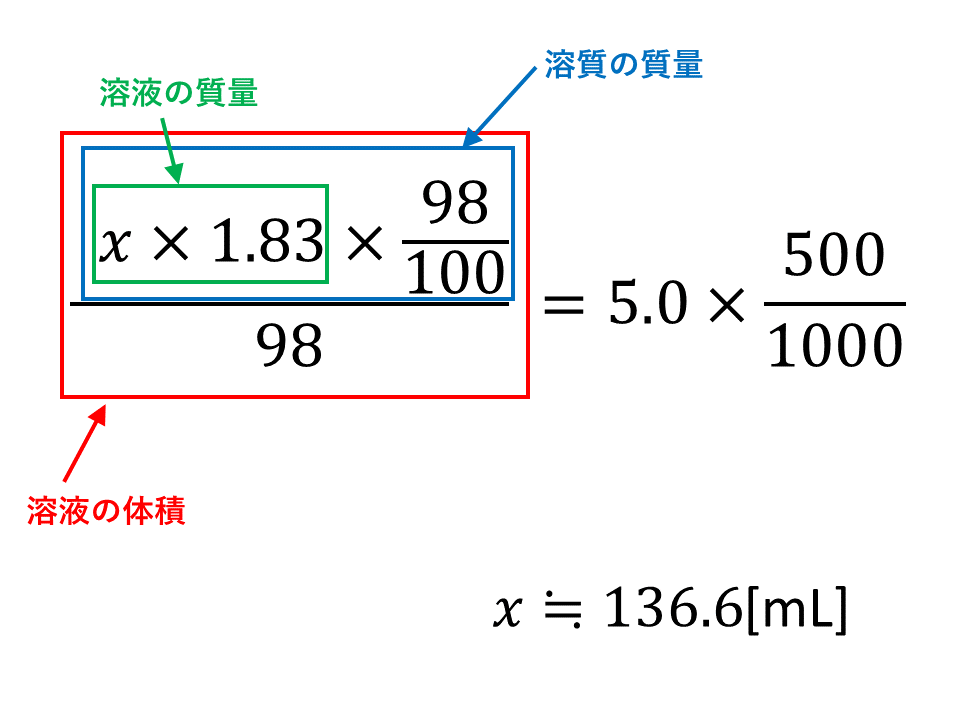
質量パーセント濃度からモル濃度への変換も同じことである。 この場合、最初に1Lあるとして計算するとよい。 質量モル濃度の考え方 さて、3番目の質量モル濃度は、 (濃度)=(溶質)÷(溶媒) として計算するので、上記の2つの濃度とは考え方が違う。 しかし、単位の変換という点 質量パーセント濃度98%、密度184 g/cm3の濃硫酸(分子量98)のモル濃度を求めよ。小数点第一位まで求めよ。 の解き方を教えて欲しいです。 小数点第一位まで求めよ。 流れとしては、 溶液の体積x mL⇒密度で溶液の質量に変換x×1g⇒質量パーセント濃度で溶質(硫酸分子)の質量に変換x×1×(98/100)⇒硫酸の分子量で割ってモルに変換 という流れになります。




2 10 050m0l 1l 100 M Descubre Como Resolverlo En Qanda




4 6 溶液の濃度 おのれー Note
モル濃度・質量パーセント濃度・質量モル濃度!濃度計算の これを計算すると、(実際にはここまで複雑な問題は出ません) pH≒6997 、と求まります。 このpHの値は限りなく7に近い数値ですが、7を超えて塩基性にはなっていませ 質量パーセント濃度 質量パーセント濃度 とは、その名の通り濃度換算ツール 質量パーセント濃度、モル濃度、規定度の換算ツールです。 換算種類と物質を選択し、比重と数量の情報を記入した上で換算するボタンを押してください。 このページのトップへ mol%とは「物質量(モル)で考えたときの濃度」のことです。 mol%は「モルパーセント」と読むことが多いです。 モルパーセントは、 溶質(溶かしている物質)のモル $\div$ 全体のモル で計算できます。 例えば、2mol の物質Aと、8mol の物質Bを混ぜてできた混合液における、物質Aのmol%は、 $2\div




質量パーセント濃度に関する問題です までは自力で解解くことができましたが がどう Clear




質量パーセント濃度 モル濃度の変換方法を攻略しよう 化学 アイドル好きのホームページ
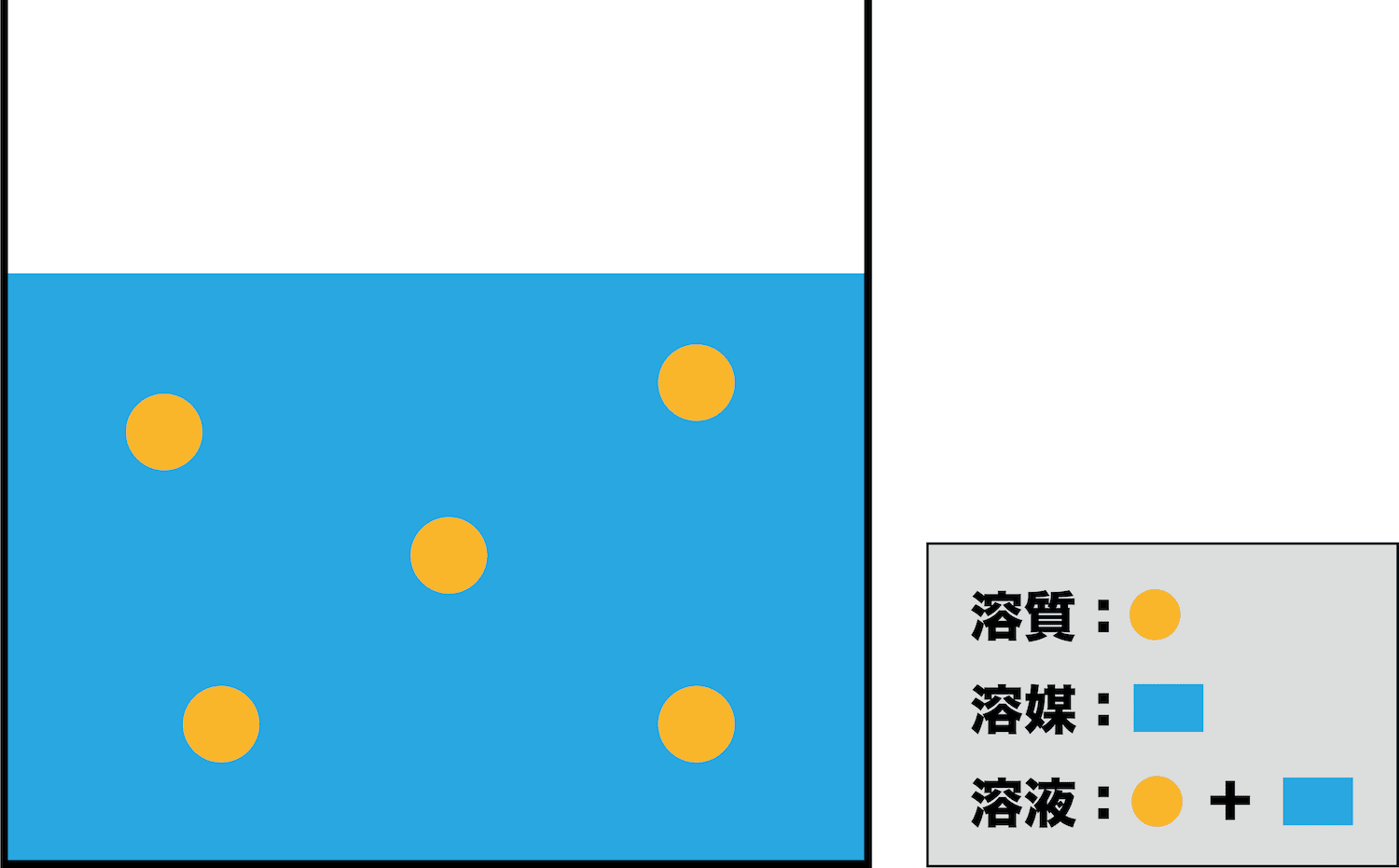
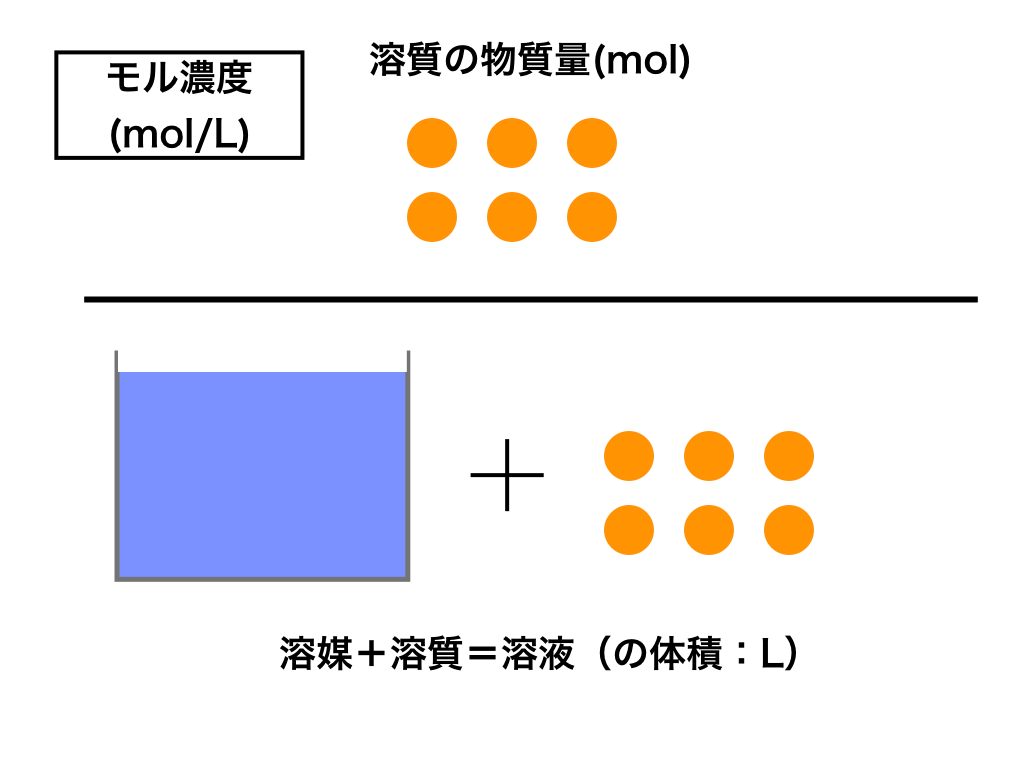
水酸化ナトリウムの質量パーセント濃度をモル濃度に変換します。 0 % 以上 522 % 以下の誤差(標準偏差)は ± mol/L です。 質量パーセント濃度 モル濃度とは、「溶液1 L中に溶けている溶質のmol」を表した濃度です。 これに対し、質量%濃度は「溶液100 g中に溶けている溶質のg」を表しています。 つまり、溶液については L ⇄ g 、溶質については mol ⇄ g の変換が必要だということです。 求めたいのは濃硫酸のモル濃度だから、 溶質 ののモルと 溶液 のリットルを求めればok!




モル濃度とパーセント濃度を脳みそを使わず変換する計算法 化学受験テクニック塾




質量 モル 濃度 どうして質量モル濃度なのか Amp Petmd Com
5% 19% Q3 モル濃度とは、どのような濃度か? 溶液の質量に対する溶質の質量をパーセントで表した濃度 溶液 1L の中に溶けている溶質の物質質量パーセント濃度(%)= 溶質の質量(g)÷ 溶液(溶質溶媒)の質量(g)×100 モル濃度(mol/L)= 溶質の物質量(mol) ÷ 溶液の体積(L) 原子量が問題文に記載されていれば、物質量(mol)と質量(g)の変換が可能で、密度が問題文に記載されていれば質量パーセント濃度とモル濃度の変換が可能です。 1 2 ①質量パーセント濃度は 72 g / 102 g = ・・・ ≒ 69 % ②グルコースのモル質量は 100 * 6 1008 * 12 * 6 = g/mol 従って、72 g のモル数は 72 g / g/mol = ・・・ ≒ 0040 mol モル濃度は「単位体積(1 L)中の溶質のモル数」な



気体の溶解度




4 6 溶液の濃度 おのれー Note
質量パーセント濃度 = 溶質 (g) 溶液 (g) ×100 なので 質量パーセント濃度 = 42 600 ×100 = 7 答7% 濃度のはなし~中学生向け 質量パーセント濃度について~ 21年2月1日 学習内容解説ブログサービスリニューアル・受験情報サイト開設のお知らせ 学習内容解説ブログをご利用下さりありがとうございます。 開設以来、多くの皆様にご利用いただいてMol/Lは、溶液1Lに溶けている物質のモル(mol)数を表します。1モルの重さは、その物質の原子量または分子量のグラム数を表します。つまり、Na 1モルの重さは、Naの原子量グラムであり23gとなります。 NaCl(585g)→Na (230g)+Cl(355g)



濃度の変換公式作ってみました 容量モル濃度 質量百分率 パーセント濃度 質量モル濃度 つれづれなる備忘録




濃度計算機 For Android Apk Download
それぞれの濃度の変換と密度 (from)質量パーセント濃度から→(to)mol濃度 解答編:質量%→mol濃度 (from)質量パーセント濃度→(to)質量モル濃度へ 解答編質量パーセント濃度とモル濃度の違い(4分10秒) モル濃度を使って混合実験(3分43秒) まとめ(1分7秒) 1/7 オープニング(31秒) 2/7 イントロ




モル濃度




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ




化学勉強法 センター試験09 Mol濃度から質量パーセント濃度へ 大村の化学勉強法




モル計算 濃度計算などの問題 解説 レベルa2 ともよし塾 受験と科学の解説授業




解説を見ても分かりませんでした 詳しく教えてください Clear




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ



質量パーセント濃度 簡単な公式で覚えよう おときち副塾長 電脳空間学習塾かもん Youtube




質量 モル 濃度 どうして質量モル濃度なのか Amp Petmd Com



濃度計算の公式 解き方 質量パーセント濃度 モル濃度 質量モル濃度 化学のグルメ




高校化学 質量パーセント濃度をモル濃度へ変える方法 Youtube




高校化学 質量と物質量 濃度の計算 オンライン無料塾 ターンナップ Youtube



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



中和滴定のモル濃度を求める課題の解き方が分かりません 写真は実験 Yahoo 知恵袋




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット
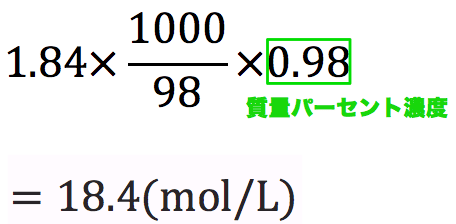



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




モル濃度から質量パーセント濃度に変えることは可能ですか Clear




質量 モル 濃度 どうして質量モル濃度なのか Amp Petmd Com




西村能一 科学の名著50冊が1冊でざっと学べる Kadokawa Na Twitteru 化学計算問題 4 濃度 Mol L Mol Kgを求める 水酸化ナトリウム25gを水100gに溶解させた溶液の密度が1 2 G Cm3であった 1 この水溶液の質量パーセント濃度は何 か 2 この水溶液



1




2 117g G 500cm3 Descubre Como Resolverlo En Qanda



Mol濃度 質量パーセント濃度 質量モル濃度の相互変換の仕方のコツ




5分でわかる モル濃度 溶液1l中に溶質が何モル溶けている 元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ



5分でわかる モル濃度と密度 質量パーセント濃度の考え方を図と練習問題付きで徹底解説 サイエンスストック 高校化学をアニメーションで理解する



2 117g G 500cm3 Descubre Como Resolverlo En Qanda




至急 質量パーセント濃度が98 の濃硫酸の密度は1 8g Cm3である この 高校 教えて Goo




この問題の考え方を教えて欲しいです Clear




モル濃度と質量パーセント濃度 化学がちょっとだけ好きな社労士




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット



モル濃度 Okedic



化学 Mol濃度 質量パーセント濃度 Youtube




モル濃度から質量パーセント濃度 Twitter Search Twitter



10倍に薄める前の食酢中に含まれる酢酸のモル濃度と質量パーセント濃度はいく Yahoo 知恵袋



1



モル濃度 質量パーセント濃度 質量モル濃度 濃度計算のコツも解説 受験メモ




質量パーセント濃度




1 M P Lihat Cara Penyelesaian Di Qanda




高校化学基礎 モル濃度の計算 練習編 映像授業のtry It トライイット




3 4mol 1l 0dfrac414 Lihat Cara Penyelesaian Di Qanda



Mol濃度 質量パーセント濃度 質量モル濃度の相互変換の仕方のコツ




4 6 溶液の濃度 おのれー Note



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ




高校化学 質量モル濃度 映像授業のtry It トライイット



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



基礎化学3 溶液



Mol濃度 質量パーセント濃度 質量モル濃度の相互変換の仕方のコツ



質量パーセント濃度28 密度1 2g Cm3の希硫酸について 2 Yahoo 知恵袋




濃度のはなし 高校生向け モル濃度と質量モル濃度について 学習内容解説ブログ




溶液の質量パーセント濃度の求め方と比重を利用した計算問題




6 7 モル濃度と密度から質量パーセント濃度を計算します 1lあったとしたら と仮定すれば あとは簡単です プレテスト化学基礎 第3問 問3 Youtube



化学基礎の問題です 質量パーセント濃度をモル濃度に換算する問題なの Yahoo 知恵袋
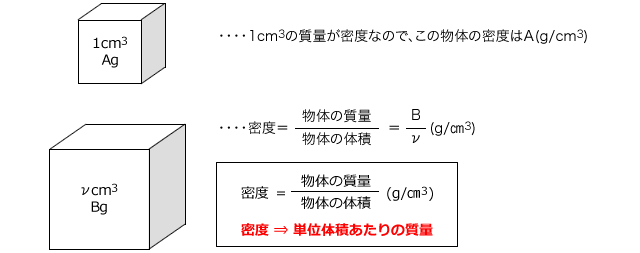



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム




4 6 溶液の濃度 おのれー Note
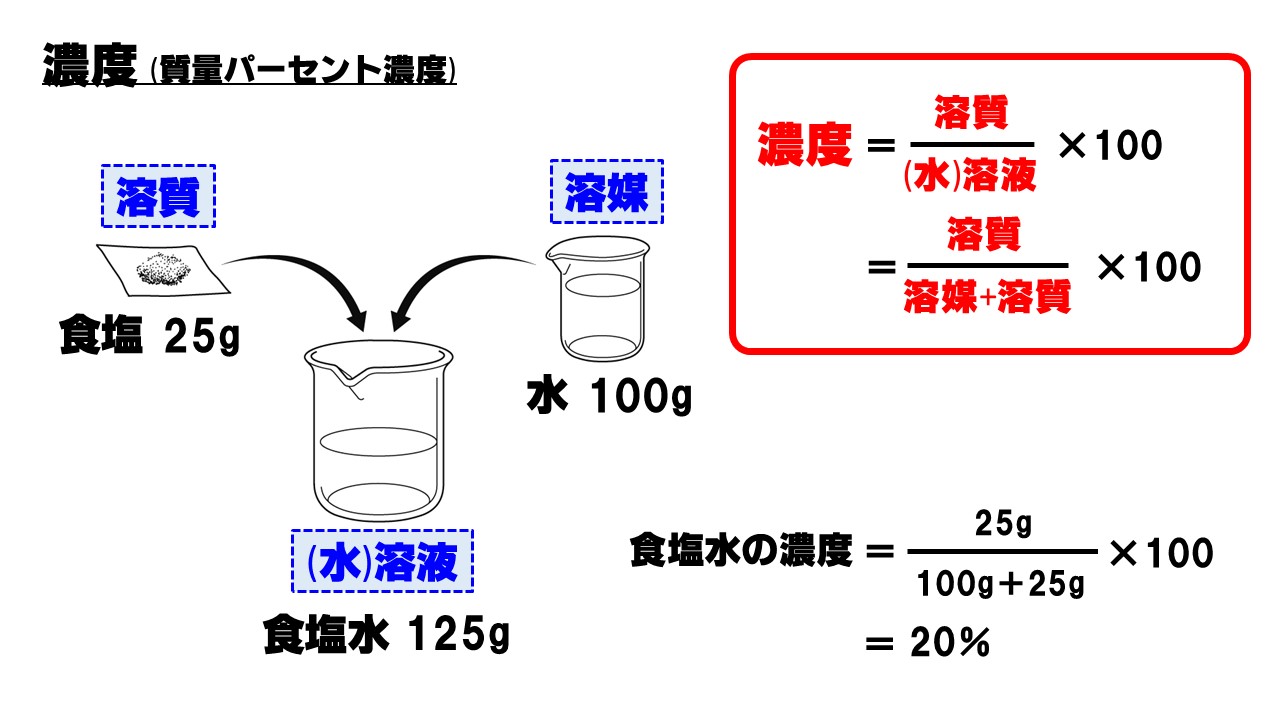



中1理科 濃度 質量パーセント濃度 のポイント Examee




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット




新商品の紹介 溶液の濃度に関する問題 完全攻略チャート 過去問解説集 数学 化学講師 佐藤学による受験生に役立つ濃縮ポイントと Etc




1分でわかる質量パーセント濃度の公式や求め方 基本を登録者数95万人人気講師がわかりやすく解説 ページ 4 4 Study Z ドラゴン桜と学ぶwebマガジン




5 98 Descubre Como Resolverlo En Qanda




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




5分でわかる モル濃度 溶液1l中に溶質が何モル溶けている 元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン



1




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット




解説を見ても分かりませんでした 詳しく教えてください Clear



受験基礎化学 18 溶液の濃度 みかみの参考書ブログ




高校理論化学 溶液の濃度と調製 質量パーセント濃度 密度とモル濃度の単位換算 受験の月




高校生 質量パーセント濃度のノート一覧 Clear



質量パーセント濃度 体積モル濃度 質量モル濃度 添付ファイルご覧くださ Yahoo 知恵袋




質量 モル 濃度 どうして質量モル濃度なのか Amp Petmd Com




質量 モル 濃度 どうして質量モル濃度なのか Amp Petmd Com
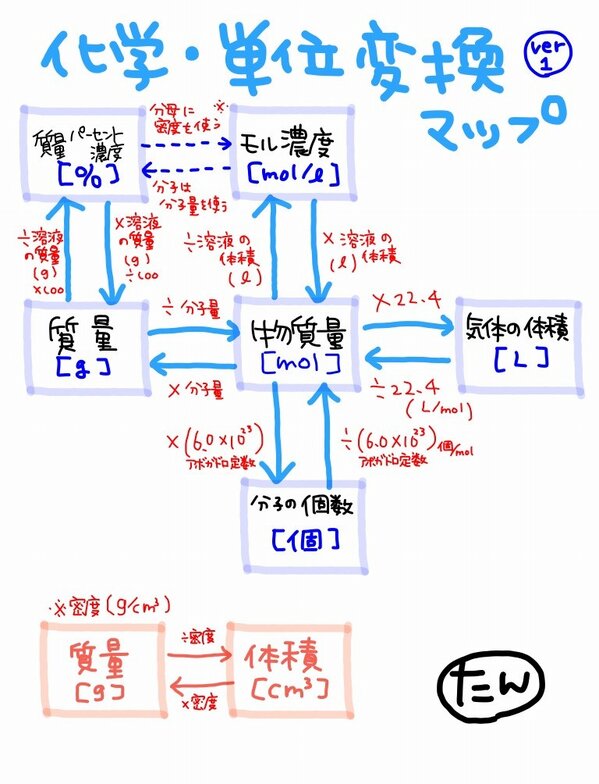



たんくん على تويتر 教えた覚えあるよー その時はモル濃度と質量パーセント濃度は別やったけどな これは少し無理やりつけた感がある Rt Hanpen52 おお 懐かしい こんなの昔頭の中にありましたね




5分でわかる モル濃度 溶液1l中に溶質が何モル溶けている 元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン




質量パーセント濃度63 の濃硝酸hno3 密度1 4 Cm 3 のモル濃度は何mol Clear




濃度について 質量パーセント W W と質量体積パーセント W v 生涯学人 まなびと 楽しいサイエンス 暮らしはサイエンス 子供たち サイエンスを感じて




溶液の濃度に関する問題 完全攻略チャート 過去問解説集 自宅でできる受験対策ショップ ワカルー Wakaru




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット




質量パーセント濃度に関する問題です 0 4がどこから出てきたのかわかりません Clear




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




高校化学基礎 硫酸とモル濃度 映像授業のtry It トライイット



Q Tbn And9gcrw0sr8fxbtv6xpolr16pkuz71aw74l2xddhh9xvrhoimgmlj L Usqp Cau




高校理論化学 食酢中の酢酸のモル濃度と質量パーセント濃度 受験の月




世界一雑な高校化学動画 モル濃度と質量パーセント濃度 Skmkchem Youtube




化学基礎 濃度変換03 Youtube




質量パーセント濃度の求め方とモル濃度の違い




質量パーセント濃度 密度で求められるのは質量ですか Clear




4 6 溶液の濃度 おのれー Note




濃度のはなし 高校生向け モル濃度と質量モル濃度について 学習内容解説ブログ




برچسب 質量パーセント濃度 در توییتر




モル濃度と質量パーセント濃度 Youtube
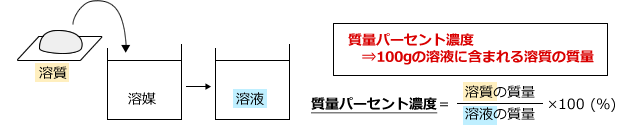



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム



0 件のコメント:
コメントを投稿